トップページ > 最新情報 > 新着情報 > 膵臓がんや予後と関連する口腔内細菌・腸内細菌種を発見
膵臓がんや予後と関連する口腔内細菌・腸内細菌種を発見
~膵がんの早期発見等のための新たな腫瘍マーカーの可能性~
2022年4月19日
東京医科大学(Tokyo Medical University)
国立国際医療研究センター(National Center for Global Health and Medicine)
欧州分子生物学研究所(European Molecular Biology Laboratory)
概 要
東京医科大学(学長:林 由起子/東京都新宿区)消化器内視鏡学分野の永田 尚義准教授と、国立国際医療研究センター(理事長:國土 典宏/東京都新宿区)消化器内科の小島 康志医長、久田 裕也医師、忌部 航医師(現:小田内科院長)、糖尿病研究センターの植木 浩二郎センター長、感染症制御研究部の秋山 徹室長、欧州分子生物学研究所の西嶋 傑、Peer Borkらの研究グループは、膵臓がん患者と非がん患者の唾液と糞便中のマイクロバイオームを網羅的に解析し、以下の知見を得ました。本研究成果は「Gastroenterology」 (IF= 22.682) のオンライン版に掲載されました(現地時間2022年4月7日公開)。
本研究のポイント
- 日本人の膵臓がん(以下、膵がん)患者に特徴的な口腔内、腸内細菌種を同定し、これらががん予測にも有用であることを示しました。さらに、日本人から同定した膵がん関連腸内細菌種が、ドイツ人やスペイン人の膵がん関連菌種と一致することを発見しました。
- 膵がんのリスク因子である膵管内乳頭粘液性腫瘍(IPMN)や慢性膵炎に関連する腸内細菌種が、膵がん関連菌種と類似していることを発見しました。
- 膵がん関連腸内細菌種を用いると、膵がんとその他の病気(糖尿病、炎症性腸疾患、大腸癌)を区別できること、また膵がんで増加する菌種は胃酸分泌抑制薬Proton-pump inhibitor (PPI)使用で増加する菌種と類似していることが判明しました。
- 腸内細菌種が膵がんの予後や抗がん剤の効果の予測に有用であることを見出しました。
- 膵がん関連の腸内細菌種に感染する新規ウイルス(ファージ)を同定しました。
今回の研究結果は、膵がん早期発見および抗がん剤治療効果予測のための新しい腫瘍マーカーの確立や、常在菌を介した膵がん発症機構の解明につながるものと期待されます。
研究の背景
膵がんは最も致死率の高い悪性腫瘍の一つであり、その罹患率は世界的に増加しています。そのため、膵がんの原因解明や早期発見に有用な非侵襲的腫瘍マーカーの同定は喫緊の課題です。人体には数百兆個・千種類以上の常在菌が消化管に生息しており、それら常在菌やウイルス(ファージ)の集合は総じて「マイクロバイオーム」と呼称され、ヒトの健康と病気を理解する上での重要な要素となっています。
今回、最新の解析技術を用いて口腔内や腸内の微生物遺伝子を網羅的に検出する事を試み、マイクロバイオームが膵がんの新たな腫瘍マーカーとして利用できる可能性を検証しました。また、世界で利用できる腫瘍マーカー同定のために、ドイツ人とスペイン人の口腔・腸内マイクロバイオームも調べ、日本人の結果と比較しました。
近年、動物実験から特定の腸内細菌種の存在が抗がん剤の効果を決定することが分かっていますが、ヒトでは十分な研究が行われていませんでした。そこで、膵がん患者において、マイクロバイオームが抗がん剤効果の予測に有用かも検証しました。
本研究で得られた結果・知見
1.膵がんに特徴的な口腔内細菌種と腸内細菌種を発見
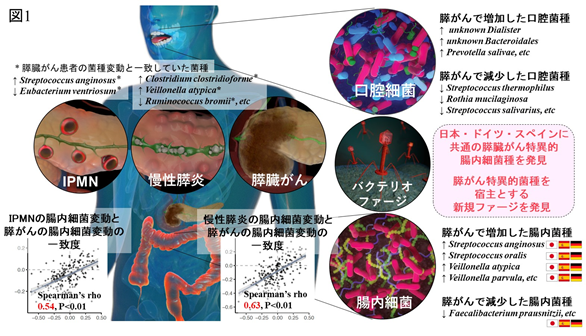
日本人の膵がん患者と、年齢、性別、患者背景因子を1:5でマッチしたコントロール症例について、唾液と糞便をショットガンメタゲノムシークエンス1)で解析しました。その結果、口腔細菌517種と腸内細菌1,151種を同定し、コントロール症例と比較することで膵がん患者に特徴的な口腔細菌18種と腸内細菌30種を発見しました。重要なことは、日本で同定した膵がん関連腸内細菌が、ドイツ人やスペイン人の膵がん関連細菌と一致することを見出したことです(図1右下)。ヨーロッパ・日本の共通菌5種のうち、膵がんで増加した4種は、通常は腸内ではまれな口腔の常在菌であること、一方、減少した1種は多くの病気でも減少が報告されており、免疫誘導と関わる菌であることが分かっています。さらに、膵がん患者で3カ国に共通して増加していた4種を宿主とする新規バクテリオファージ58種を発見しました。今回の結果は、特定の細菌の増加または減少が膵がんの発生やがん進行の原因となる可能性を示唆しており、今後それらの細菌を介した発がん機構の解明が望まれます。また、それら細菌が実際に発がんや進行の原因である場合は、それらをターゲットとするファージセラピーにより膵がんを予防または治療できる可能性があり、本研究はその基盤データを提供したことになります。
次に、膵がんで認めた特徴的な腸内細菌叢が、膵がんリスク患者群のものと類似しているのかを検証したところ、膵管内乳頭粘液性腫瘍(IPMN)や慢性膵炎の腸内細菌叢は膵がん患者のものと類似することを見出しました。また、慢性膵炎患者(相関係数0.63)の腸内細菌叢の方がIPMN患者(相関係数0.54)のものよりも膵がん患者の腸内細菌叢と類似していることも分かりました(図1下段)。他の病気についても同様の解析を行い、膵がん患者に特徴的な腸内細菌叢は、糖尿病、炎症性腸疾患、大腸がんの腸内細菌叢とは異なっており区別できるものの、胃酸分泌抑制薬であるProton-pump inhibitor (PPI)2)使用者の腸内細菌叢とは類似していることを発見しました。疫学研究で、IPMN、慢性膵炎、PPI使用は膵がんリスクと関連することが報告されており、我々の結果は、腸内細菌叢がこれらの病態と膵がんとを結びつける一つの要因であることを示唆しています。
2.膵がん予測に口腔内細菌種と腸内細菌種が有用であることを発見
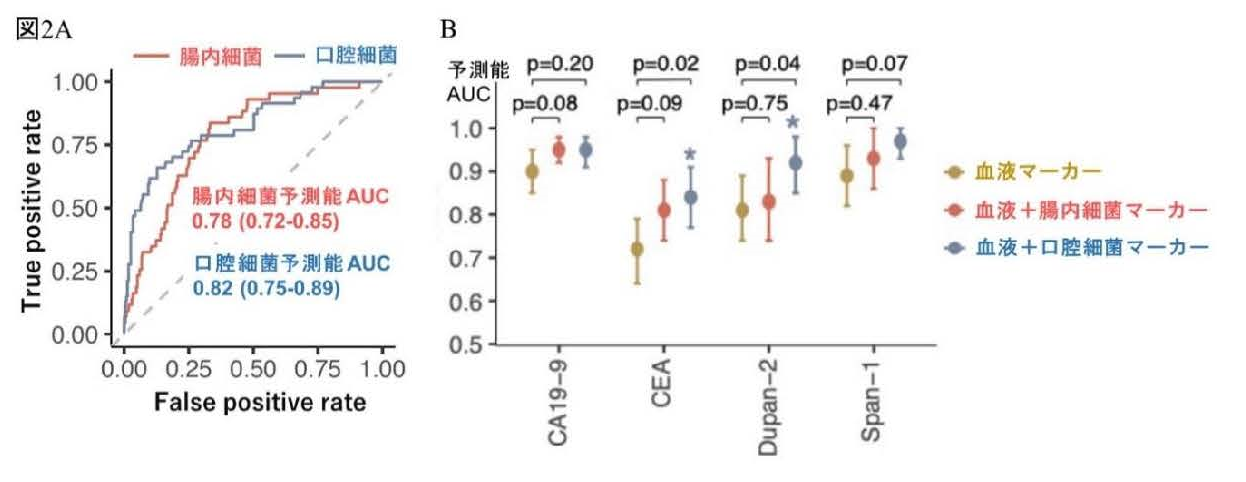
膵がんに特徴的な細菌叢が「がんの早期発見」のための腫瘍マーカーとして利用できるかを検証しました。口腔と腸内細菌叢の膨大な情報から機械学習法という解析法を用いて膵がんの予測能を調べたところ、特定の口腔や腸内細菌を数菌種用いると高い確率で膵がんを予測できることが分かりました(図2A)。さらに、従来の血液マーカー(例、CA19-9)と口腔や腸内細菌種を併用すると、血液マーカー単独よりも膵がんの予測精度が高まることを発見しました(図2B)。
3.膵がん患者の抗がん剤投与後の予後に腸内細菌種が関連することを発見
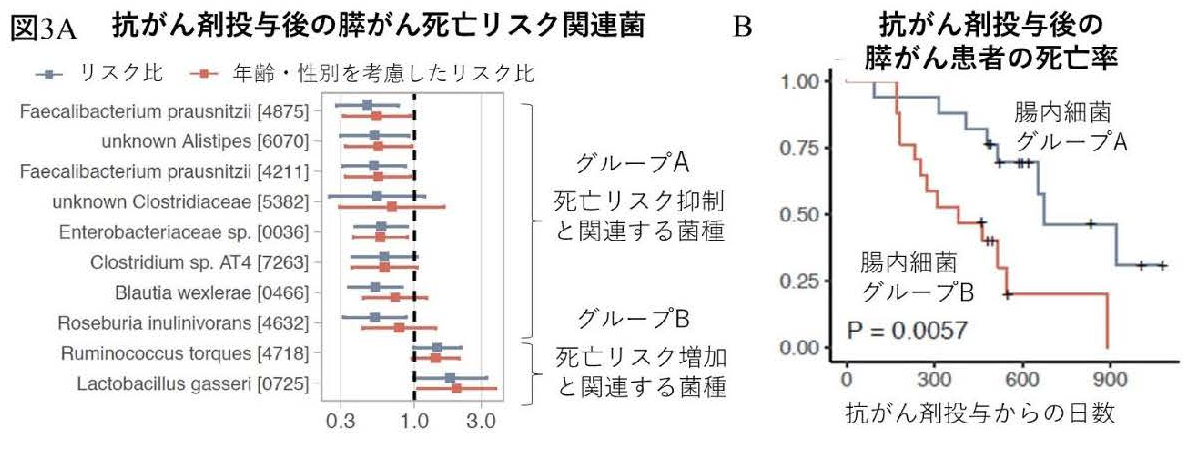
腸内細菌叢を「膵がん発見のマーカー」としてだけなく、「膵がん診断後の治療効果予測」にも利用できるのではないかと考えました。そこで、治療前に採取した糞便の腸内細菌と抗がん剤治療後の死亡率との関連を調べました。まず、腸内細菌叢を用いた死亡予測モデルを作成することで、膵がん患者を死亡リスクが低い腸内細菌叢グループAとリスクが高いグループBに分けることができました。死亡リスクが低いグループAに豊富に見られる菌種の多くは酪酸や酢酸など短鎖脂肪酸3)を産生する菌と判明しました(図3A)。実際、グループAの菌種を有する患者は、グループBを有する患者と比較し有意に抗がん剤治療後の生存率が長いことを見出しました(図3B)。短鎖脂肪酸には免疫の恒常性を保つ働きがあることが分かっており、グループAの菌種の存在が宿主の免疫応答を調整することで予後良好な結果になっている可能性が示唆されました。
今後の研究展開および波及効果
本研究の成果から、マイクロバイオームをマーカーとして膵がんの早期発見や抗がん剤の治療効果予測に利用できる可能性が明らかとなり、膵がんや予後のハイリスク患者の絞り込みから膵がん診療における個別化医療の実現が期待できます。また、従来の血液腫瘍マーカーと唾液や糞便マーカーと組み合わせることで、より早期の膵がん発見が可能となり、治療率向上と予後改善が期待されます。さらに、膵がんに特異的な腸内細菌に感染するバクテリオファージの同定は、がんの発生や進行を抑制することを目指したファージセラピー4)の研究開発を促進させます。
掲載誌名・DOI
- 掲載誌名:Gastroenterology
- DOI:10.3892/ijo.2022.5344
- 掲載誌 URL:https://www.gastrojournal.org/article/S0016-5085(22)00354-7/fulltext#relatedArticles
- DOI: https://doi.org/10.1053/j.gastro.2022.03.054
論文タイトル
Metagenomic identification of microbial signatures predicting pancreatic cancer from a multinational study
著者
Naoyoshi Nagata*, Suguru Nishijima*, Yasushi Kojima, Yuya Hisada, Koh Imbe, Tohru Miyoshi-Akiyama, Wataru Suda, Moto Kimura, Ryo Aoki, Katsunori Sekine, Mitsuru Ohsugi, Kuniko Miki, Tsuyoshi Osawa, Kohjiro Ueki, Shinichi Oka, Masashi Mizokami, Ece Kartal, Thomas S. B. Schmidt, Esther Molina-Montes, Lidia Estudillo, Nuria Malats, Jonel Trebicka, Stephan Kersting, Melanie Langheinrich, Peer Bork, Naomi Uemura, Takao Itoi, and Takashi Kawai
永田 尚義*, 西嶋 傑*, 小島 康志, 久田 裕也, 忌部 航, 秋山 徹, 須田 亙, 木村 基, 青木 亮, 関根 一智, 大杉 満, 三木 邦寿, 大澤 毅, 植木 浩二郎, 岡 慎一, 溝上 雅史, Ece Kartal, Thomas S. B. Schmidt, Esther Molina-Montes, Lidia Estudillo, Nuria Malats, Jonel Trebicka, Stephan Kersting, Melanie Langheinrich, Peer Bork, 上村 直実, 糸井 隆夫, 河合 隆(*責任著者)
主な競争的研究資金
本研究は、日本学術振興会科学研究費助成事業 基盤研C JP17K09365(代表:永田 尚義)、日本膵臓病研究財団(代表:永田 尚義)、上原記念生命科学財団(代表:永田 尚義)、国際医療研究開発費19A1011(代表:小島 康志)、19A-2015(代表:木村 基)、29-1025(代表:忌部 航、久田 裕也、関根 一智)の支援を受け実施しました。
補足資料:図解・表等 添付
- ショットガンメタゲノムシークエンス:サンプル中の微生物を単離や培養することなく、DNA集合体を網羅した状態でゲノム配列を解読することである。16S rRNAシークエンスとは異なり、全ゲノム配列を対象とするため、より精度の高い菌種組成の解明が可能である。また、16S rRNA解析では困難であった、菌叢の持つ機能・代謝遺伝子、細菌だけでなく、古細菌、バクテリオファージ、真菌なども解析可能である。
- Proton-pump inhibitor (PPI):胃粘膜の壁細胞には胃酸分泌を行うプロトンポンプというタンパク質があり、そのポンプを阻害すると胃酸分泌が強力に抑えられる。プロトンポンプ阻害剤には、胃酸分泌を抑えることで胃潰瘍や逆流性食道炎などに伴う症状を改善し、再発を抑制する効果がある。商品名として、オメプラール、オメプラゾン、タケプロン、パリエット、ネキシウムなどがある。なお、タケキャブはPPIとは異なる作用でプロトンポンプを阻害する薬剤であるが、腸内細菌の変化はPPIとほぼ同等である。
- 短鎖脂肪酸:腸内細菌が産生する、酪酸、プロピオン酸、酢酸などの有機酸のこと。ヒトの免疫の恒常性を保つ作用(抗炎症作用)を持つほか、腸上皮細胞のエネルギー源となり、さらに腸管粘膜で抗微生物効果を示すなど、ヒトにおいて優れた生理効果を発揮することが分かっている。がん患者や炎症性腸疾患患者ではこの短鎖脂肪酸産生と関与する菌群が共通して減少している。
- ファージセラピー:細菌に感染するウイルス(ファージ)を用いた治療のこと。抗生物質の使用が薬剤耐性菌の出現と蔓延を引き起こしている今日において、抗生物質を用いずに特定の菌種(薬剤耐性菌や疾患と関連する菌)を消失・抑制が見込める治療として注目が集まっている。すでにロシア、ジョージア、ポーランドでは製剤化されており、重大な毒性や副作用なしにヒトでの応用が成功しているが、今後臨床研究によるさらなる効果や安全性の情報が期待される。
本研究に関する問い合わせ先
- 東京医科大学 消化器内視鏡学分野
准教授 永田 尚義
TEL:03-3342-6111(病院代表)
E-mail:n-nagata@tokyo-med.ac.jp
プレスリリースに関するお問い合わせ
- 学校法人東京医科大学 企画部 広報・社会連携推進室
TEL:03-3351-6141(大学代表)
E-mail:d-koho@tokyo-med.ac.jp - 国立研究開発法人 国立国際医療研究センター(NCGM)
広報企画室 西澤
TEL:03-3202-7181(代表)
E-mail:press@hosp.ncgm.go.jp